
- 00Días
- 00Horas
- 00Minutos
- 00Segundos

El ácido benzoico es un ingrediente muy utilizado como conservante en cosmética natural, y es por eso, que hemos decido dedicarle un post, de esta forma podréis conocer mucho mejor este ingrediente, y aprender a utilizarlo en vuestras formulaciones.
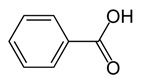
A nivel químico, el ácido benzoico (INCI: Benzoic Acid), es un compuesto que comprende un núcleo formado por un anillo de benceno unido a un ácido carboxílico. Su fórmula molecular es C 7 H 6 O 2, que también puede ser expresada como C6H5COOH. Se trata de un sólido cristalino incoloro, que normalmente se comercializa en forma de polvo, y es el ácido carboxílico aromático más simple. Además de la forma ácida, el ácido benzoico se puede encontrar en forma de sal, como benzoato de sodio (INCI: Sodium Benzoate).
En la naturaleza, el ácido benzoico se puede encontrar en forma de ésteres en muchas especies de plantas y animales. Se han encontrado cantidades apreciables en la mayoría de las bayas (alrededor de 0.05%) y especialmente en los arándanos.
El ácido benzoico a pesar de ser un ácido muy estable, se puede inactivar por combinación con tensoactivos no iónicos y aumentando el pH de la formulación final por encima de 5.00. Se inactiva también por compuestos de amonio cuaternario, sales cálcicas y férricas, caolín, proteínas y glicerol. Combinado con ácido ascórbico puede formar benceno, el cual es perjudicial para la salud.
Tiene un punto de fusión de 122,4ºC. Es un producto fotosensible, y hay que protegerlo de la luz.
La sal sódica se disuelve en agua hasta un 55%, no obstante, la forma ácida sólo es soluble hasta el 0,2%. Esta solubilidad de la forma ácida aumenta cuando se lleva a ebullición. Por otra parte, el ácido benzoico es soluble en aceite y en etanol, mientras que la sal sódica no.
A la hora de formular un producto cosmético natural utilizando ácido benzoico, será importante tener en cuenta el pH final de la formulación, ya que dependiendo de este habrá más o menos proporción de la forma ácida, que es la forma activa, es decir, se verá afectada su actividad como conservante. El ácido benzoico tiene un pKa de 4,18, y el porcentaje en forma ácida a diferentes valores de pH será el siguiente:
| pH | 3 | 4 | 5 | 6 | 7 |
| % en forma activa | 94,0 | 61,0 | 13,0 | 1,5 | 0,0 |
Es necesario que la formulación tenga un pH por debajo de 3 para que se manifieste su total actividad. Como esta premisa es difícil de cumplir en cosmética natural, se recurre a la combinación con otros conservantes, manteniendo siempre un pH máximo de 4,5 para mantener cierta actividad. Sobre todo es un conservante con alta actividad fungicida, pero también tiene eficacia antibacteriana, aunque es de carácter pobre frente a pseudomonadáceas.
El ácido benzoico y su sal sódica están permitidos en la UE a una concentración del 2,5% en su forma ácida en productos que se enjuagan (a excepción de los productos bucales). En los productos bucales, está permitido a una concentración del 1,7%, y en los productos que no se enjuagan a una concentración máxima de 0,5%. Si la sal no es de sodio o es un éster, el máximo admitido es de un 0,5% (en forma ácida) en todos los productos. En Japón está permitido a un 0,2% como ácido y a un 1% como sal sódica.
El ácido benzoico es moderadamente irritante para la piel, e irritante para los ojos, aunque la sal sódica no. Ninguno de los dos compuestos tiene capacidad de sensibilización en los animales pero se han observado reacciones positivas en humanos mediante patch tests. Se cree que estas reacciones son debidas a urticaria de contacto, de origen no inmunológico (opinión SCCP/0891/05). La conclusión del CICAD (Concise International Chemical Assessment Document) sobre estas sustancias es que provocan reacciones de contacto no inmunológicas, y que este efecto puede pasar desapercibido en personas sanas pero en personas con asma o con urticaria frecuente puede exacerbar los síntomas, se piensa que por mecanismo colinérgico. Según este mismo Organismo, se deberían tener en cuenta estos datos si se formulan productos para niños.

Para saber más sobre conservación en nuestra escuela puedes encontrar el curso en certificación en conservación natural dónde podrás aprender más sobre ingredientes conservantes y otros temas relacionados con la conservación.
1. Ácido benzoico | C6H5COOH – PubChem [Internet]. [cited 2020 Jul 20]. Available from: https://pubchem.ncbi.nlm.nih.gov/compound/Benzoic-acid#section=CAS
2. Reglamento (CE) n o 1223/2009 del Parlamento Europeo y del Consejo, de 30 de noviembre de 2009, sobre los productos cosméticos (Texto pertinente a efectos del EEE). Disponible en: https://eur-lex.europa.eu/eli/reg/2009/1223/oj/spa
3. Scientific Committee on Consumer Products. 2005. Opinion on benzoic acid and sodium benzoate. Brussels. European Comission.
4. Archivo: Benzoic acid.png – Wikimedia Commons [Internet]. [consultado 24 julio 20204]. Dusponible en: https://commons.wikimedia.org/wiki/File:Benzoic_acid.png
5. Cosmetic ingredient database | Internal Market, Industry, Entrepreneurship and SMEs [Internet]. [cited 2020 Jul 24]. Available from: https://ec.europa.eu/growth/sectors/cosmetics/cosing_en
6. Leranoz S, Orús P. Sociedad Española de Microbiología. Microbiología y conservación en cosméticos.
Escrito por María Cerdán.





Compras 100% seguras con:
![]()

Compras 100% seguras con:
![]()
¿Tienes alguna duda? Te llamamos gratis y sin compromiso. Déjanos tu teléfono y nos podremos en contacto contigo a la mayor brevedad.
Nuestro horario de atención es de 9:00 a 15:30 CEST