
- 00Días
- 00Horas
- 00Minutos
- 00Segundos

El PIF (Product Information File) o expediente de información de producto es un paso necesario a la hora de poner nuestro producto cosmético en el mercado. Así viene recogido en el Reglamento europeo 1223/2009 sobre productos cosméticos. En este Reglamento también se indica que es el responsable de la puesta en el mercado (al que llamamos fabricante) el que debe asegurar el cumplimiento del este Reglamento, garantizando la seguridad y la calidad del producto.
¿Y qué debemos hacer antes de la puesta en el mercado de mi producto?
Básicamente son tres pasos:
En este artículo centraremos nuestra atención en el PIF y su contenido.
El Expediente de Información del Producto (PIF) se debe realizar para cada producto cosmético puesto en el mercado. Se debe mantener durante los diez años siguientes a la fecha en la que el último lote del producto cosmético se pone en el mercado.
El Reglamento nos dice en su Artículo 10 que el Expediente debe tener lo siguiente:
Bien visto esto es fácil… total, son 5 cosas… pero hay que ir un poco más adelante.
Por ejemplo, para realizar la evaluación de seguridad nos tenemos que ir hasta el Anexo I. Este Anexo nos indica que la persona que realiza esta evaluación necesita revisar para su informe una serie de documentos relacionados con el producto cosmético, los ingredientes y con el modo de uso y población a la que se dirige el producto.
Para facilitar el trabajo, nosotros vamos a dividir el expediente (PIF) en 3 partes.
Una Administrativa, una para los Ingredientes y la última, la relacionada con el propio Producto Acabado.
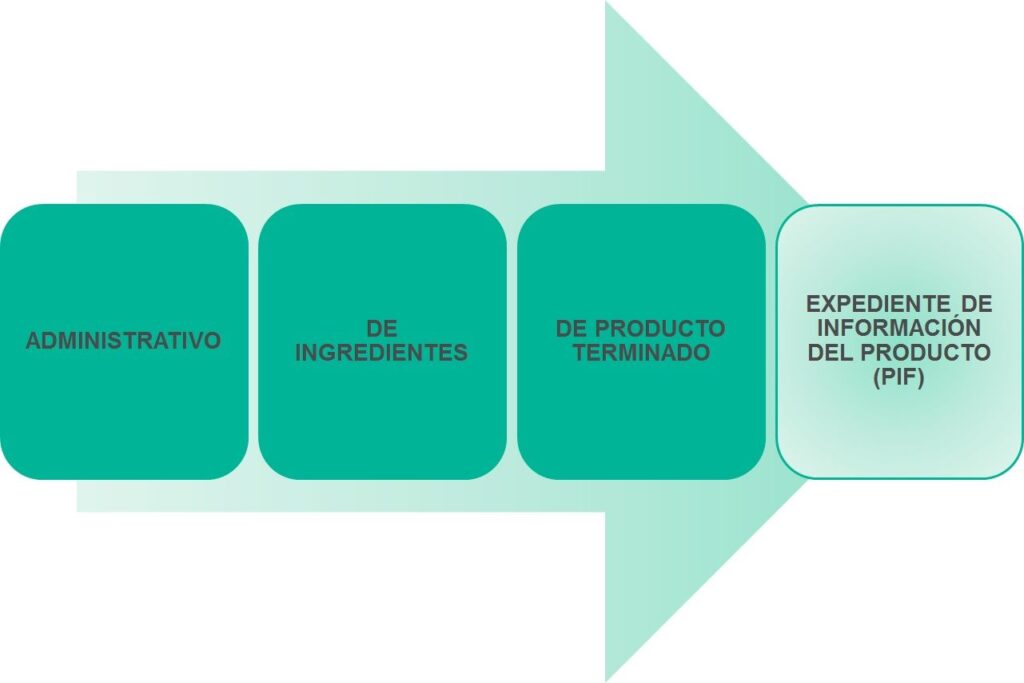
Tendrá las siguientes partes que incluirán:
DATOS DEL PRODUCTO
ETIQUETADO. Resumiendo lo que debe incluir,
(*) en el idioma del consumidor.
NOTIFICACION A LA COMISIÓN EUROPEA a través del CPNP (Cosmetic Products Notification Portal). CPNP tiene como finalidad facilitar la presentación de la información sobre los productos que se ponen en el mercado europeo. Esta información es crucial tanto para los centros de toxicología, ya que así pueden tratar rápidamente las eventuales intoxicaciones, como para las autoridades nacionales, que podrán realizar un mejor control del mercado.
EVALUACION DE LA SEGURIDAD o CPSR (Cosmetic Product Safety Report). La premisa básica de los productos cosméticos que se comercializan en Europa es que sean seguros. La evaluación de la seguridad es el informe que realiza el responsable y que debe demostrar la seguridad del cosmético cuando se utilicen en las condiciones normales o razonablemente previsibles de uso.
ESPECIFICACIONES DE LAS MATERIAS PRIMAS La información sobre las características físico-químicas y microbiológicas de cada uno de los ingredientes.
Se deberá poner especial atención a aquellos ingredientes que se encuentren en los Anexos del Reglamento: colorantes, conservantes, filtros solares y sustancias restringidas.
HOJAS DE SEGURIDAD o Material Safety Data Sheet (MSDS) de todas las materias primas, actualizada.
DATOS DEL PERFUME: debe incluir nombre y número de código del perfume e identidad del proveedor. La hoja de seguridad (MSDS), la declaración alérgenos y el certificado IFRA.
La declaración de alérgenos nos va a permitir calcular aquellos que deberemos indicar en nuestra lista de ingredientes. IFRA son las siglas de International Fragrance Association. Ésta garantiza la seguridad de los ingredientes utilizados en el perfume para las personas y para el medio ambiente. Actualmente está en vigor la edición 49.
FÓRMULA cualitativa y cuantitativa del producto acabado con: Identidad química de las sustancias (INCI, CAS). El INCI es la nomenclatura utilizada en Europa para designar cada ingrediente (siglas de International Nomenclature of Cosmetic Ingredients). El CAS es una identificación numérica única para los ingredientes químicos. Sus siglas corresponden a CAS Registri Number Función prevista de cada uno de los ingredientes. Lista de ingredientes.
ESPECIFICACIONES FÍSICO-QUÍMICAS Y MICROBIOLÓGICAS del producto acabado. Con aquellos análisis que vamos a realizar al producto para la liberación de cada lote.
ESTABILIDAD físico-química y microbiológica del producto acabado. Deberemos incluir aquí el informe del estudio de estabilidad que hayamos realizado y que nos va a proporcionar la justificación de la caducidad.
JUSTIFICACIÓN DEL PAO, de acuerdo bien a su estudio empírico, bien al cálculo de acuerdo con las Guías publicadas por entidades como la AFSSAPS, Agencia Francesa de la Salud.
CHALLENGE TEST. Se incluirán los resultados del ensayo de eficacia del conservante que garantizan que el producto está realmente bien conservado. Para productos de bajo riesgo de contaminación microbiológica, para los que no se considere necesario realizar el Challenge test deberá incluirse al menos, el estudio de la Actividad de agua (Aw) que justificará que la fórmula no es susceptible de sufrir contaminación microbiana.
INFORMACIÓN SOBRE EL MATERIAL DE EMBALAJE que está en contacto con el producto, es decir, el embalaje primario (tubo, tarro…). Se deben incluir aquí los ensayos realizados para comprobar la compatibilidad entre tarro/bote/tubo y producto, como la ausencia de pérdidas, de rotura de las tapas, etc.
ESTUDIOS DE SEGURIDAD. Estudios realizados in vitro e in vivo que confirmen la compatibilidad y aceptabilidad del producto cosmético. Pueden ser, por ejemplo, irritación ocular, patch test, test de uso bajo control médico…
MÉTODO DE FABRICACIÓN. CERTIFICADO DE CUMPLIMIENTO DE BPF. Incluir el método de fabricación del producto, así como una confirmación del cumplimiento con las Buenas Prácticas de Fabricación (BPF).
La Norma que aplica es la ISO 22716. Se puede incluir la copia de la Certificación ISO. Pero como no es necesario estar certificados, se puede incluir un Certificado firmado por el fabricante que confirme que se fabrica siguiendo dicha norma.
ESTUDIOS DE EFICACIA. Son todos los estudios que deben demostrar los efectos reivindicados en el etiquetado. Estos estudios pueden ser objetivos, realizados con instrumental y técnicos que realizan las lecturas e interpretación de datos, como una prueba de hidratación, de medida de las arrugas y/o subjetivos como son los cuestionarios a consumidores (test de uso), que nos dan su opinión respecto de diferentes particularidades del producto: permite hacer afirmaciones como “el 75% de usuarios opina que la piel queda sedosa”.
DATOS DE EFECTOS NO DESEADOS si es un producto que ya se ha comercializado deberán incluirse el máximo de datos posible sobre las reclamaciones que ha tenido vs el número de unidades vendidas. Este dato es el mejor indicador de la seguridad que tiene un producto.
En caso de que el producto sea nuevo, deberemos incluir un escrito conforme vamos a mantener un sistema de vigilancia según las directrices de la UE para la comunicación de efectos graves no deseados.

El expediente puede estar en un soporte papel o informático. Lo importante es tenerlo accesible a petición de las Autoridades. Es importante que el expediente se encuentre en la lengua oficial del país o como mínimo, en una fácilmente inteligible para las Autoridades competentes.
Os recomendamos ordenar en una plantilla, estructura en carpetas o como más cómodos os sintáis esta información. A partir del primer expediente realizado será mucho más sencillo.
Aprende sobre formulación y regulación de cosmética natural en nuestros cursos. ¡Empieza hoy!
Escrito por Mentactiva.





Compras 100% seguras con:
![]()

Compras 100% seguras con:
![]()
¿Tienes alguna duda? Te llamamos gratis y sin compromiso. Déjanos tu teléfono y nos podremos en contacto contigo a la mayor brevedad.
Nuestro horario de atención es de 9:00 a 15:30 CEST